こんにちは。理科教師の試薬35です。
皆さんは、切ったまま置いておいたリンゴが茶色く変色してしまったのを見たことはありませんか?
他にも、ピカピカだった10円玉がいつの間にか黒ずんでいたり、公園の鉄棒が赤茶色のサビでザラザラになっていたり。
これらはすべて、化学の世界では**「酸化(さんか)」**と呼ばれる現象です。物質が、空気中の「酸素」とくっつくことで起こります。
でも、ここで一つ不思議なことがありませんか?
同じように空気(酸素)に触れているし、水にも濡れるのに、キッチンのシンク(ステンレス鋼)は、なぜいつまでもピカピカで錆びないのでしょうか?
今回は、前回の記事で第3位にランクインした不憫な元素「ニッケル」の活躍も交えながら、ステンレスが錆びない「逆転の発想」について紐解いていきましょう。
そもそも「錆びる」とはどういうこと?

鉄が錆びてボロボロになるのは、鉄の表面からどんどん酸素が入り込み、中まで「酸化鉄(サビ)」に変わってしまうからです。
では、このサビを防ぐにはどうすればいいでしょうか?
シンプルに考えれば**「鉄に酸素を触れさせないこと」**ですよね。
「ペンキを塗ってコーティングする!」と考えた方、大正解です。鉄棒にペンキが塗られているのはそのためです。でも、ペンキは剥がれたらそこから錆びてしまいます。キッチンのシンクにペンキを塗るわけにもいきません。
そこで、昔の科学者たちはとんでもない**「逆転の発想」**を思いつきました。
錆びないために「あえて先に錆びさせる」
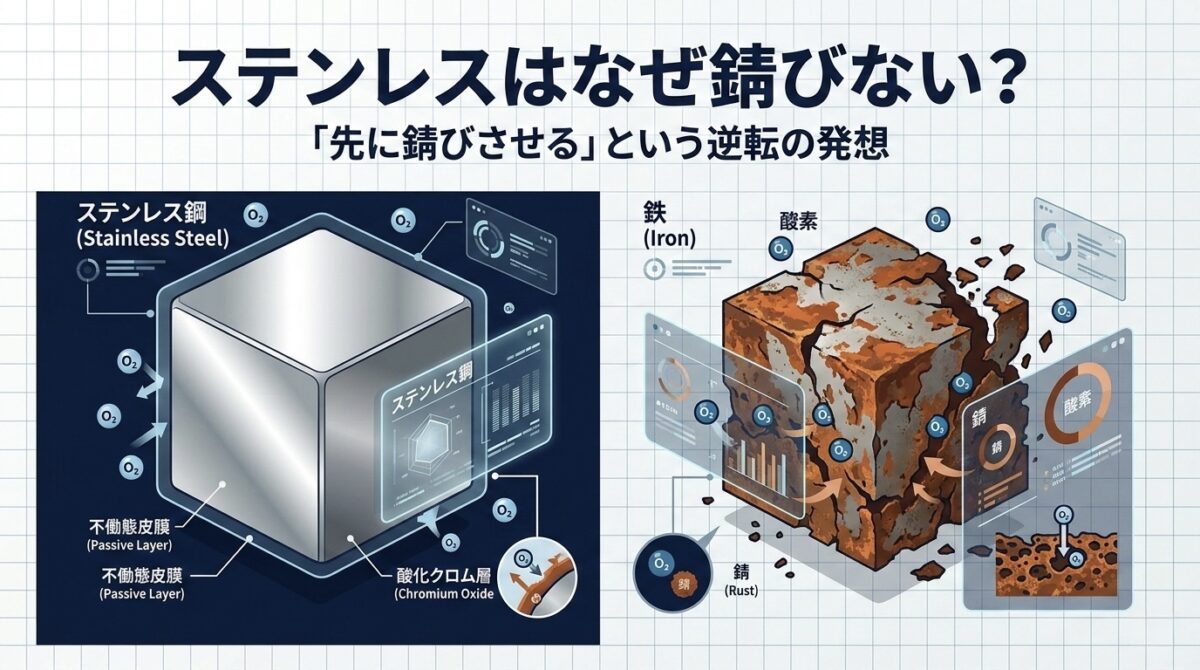
「どうせ酸素とくっついて錆びてしまうなら、中までボロボロになる前に、表面だけを一瞬で『めちゃくちゃ薄くて硬いサビ』にしてしまえばいいのではないか?」
……驚きますよね。これがステンレス鋼(Stainless Steel=サビのない鉄)の最大の秘密です。
鉄に**クロム(Cr)**という元素を混ぜておくと、空気に触れた瞬間に、表面にわずか数ナノメートル(1ミリの100万分の1)という極薄の膜が張られます。この膜は「不動態皮膜(ふどうたいひまく)」と呼ばれる、目に見えない透明なバリアです。
実はこのバリア自体が、クロムが酸素とくっついてできた**「緻密なサビ」**なのです。
表面が超強力なサビのバリアで完全に覆われるため、それ以上は酸素が中に入り込めず、結果として鉄そのものはいつまでもピカピカな状態を保てるというわけです。
最強の相棒「ニッケル」の妥協なき守り

さて、ここで前回の記事に登場したニッケル(Ni)の出番です。
昔の人に「銅の偽物だ!」と八つ当たりされ、「悪魔の銅」という不名誉な名前の由来を持っていたニッケル。その特徴は「他のものとくっついたら、しぶとくてなかなか離れない」ことでした。
ステンレス鋼を作る際、鉄とクロムに加えて、このニッケルを混ぜ合わせます(これがシンクなどに使われる代表的なステンレスです)。すると、どうなるでしょうか?
ニッケルの「しぶとく結びつく」という性質が、透明なバリアをさらに強力で安定したものにアップグレードしてくれるのです。たとえ包丁などで表面のバリアが傷ついても、空気中の酸素と素早く結びつき、瞬時にバリアを自己修復してしまいます。
「偽物」と罵られたニッケルの頑固さが、今では私たちの生活を支える「絶対にサビを許さない最強の盾」として活躍しているのです。
おわりに
いかがでしたでしょうか。
「酸化=物質が劣化する悪いこと」というイメージがあったかもしれません。しかし、その酸化という現象を逆手にとり、「先に強力なサビのバリアを作る」ことで本体を守り抜く。このステンレスの仕組みを知ると、見方が少し変わりませんか?
一見すると弱点やマイナスに思える性質(酸化しやすいこと、頑固でしぶといこと)も、組み合わせや考え方次第で、誰も予想しなかったような「強み」へと生まれ変わります。科学の世界におけるこうしたプロセスは、私たちの日常や生き方にも、少しだけヒントをくれているような気がします。

コメント